
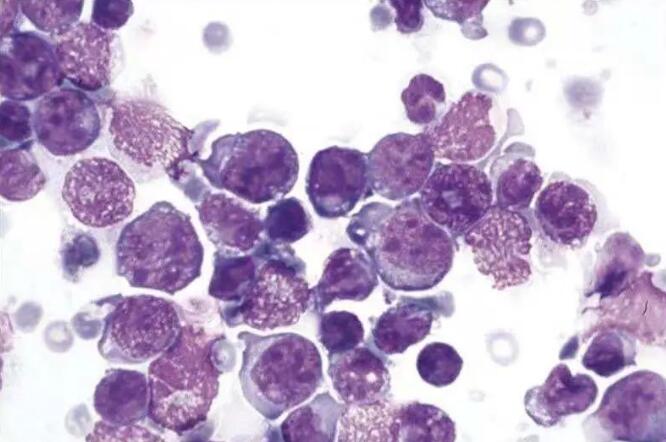
历史上,艾滋病毒感染者患非霍奇金淋巴瘤的风险较高。
根据NCI主导的一项研究,他们也比没有艾滋病毒的人更有可能死于这种疾病。
抗逆转录病毒疗法的普及和更有效的癌症治疗降低了死于艾滋病毒相关恶性肿瘤的人数比例。然而,根据NCI的另一项分析,非霍奇金淋巴瘤仍然是艾滋病毒感染者癌症死亡的主要原因(3.5%)。
这些人中的许多人发展出治疗耐药性疾病,需要的不仅仅是传统的化学免疫疗法。
嵌合抗原受体T细胞是治疗高风险和晚期非霍奇金淋巴瘤的重大进展;然而,到目前为止,还没有HIV感染者有资格通过临床试验接受研究性CAR-T治疗。其他患者由于缺乏保险或因感染艾滋病毒而被制造商禁止而无法获得治疗。
宾夕法尼亚大学佩雷尔曼医学院临床医学副教授、艾布拉姆森癌症中心t细胞淋巴瘤项目主任Stefan K. Barta医学博士告诉Healio |细胞治疗Next说:“人们仍然认为艾滋病毒感染者更容易受到感染并发症的影响,因此,甚至不应该对某些更强化的[癌症]治疗进行评估。不成比例的艾滋病毒感染者来自代表性不足的少数群体,因此显然也存在获得护理的问题。”
1. 初步数据
在将CAR-T疗法推广到艾滋病毒感染者之前,有必要开展研究,确认CAR-T疗法对免疫功能低下患者的安全性和有效性。
然而,由于这些个体被禁止注册试验,这方面的数据很少。
在去年的ASH年会上发表的一项小型回顾性研究的结果首次表明,CAR - t细胞疗法对艾滋病毒感染者同样有效,而且没有带来额外的安全风险。
该研究由艾滋病恶性肿瘤联盟(AMC)和国际血液和骨髓移植研究中心(CIBMTR)的成员进行,包括27例患者(中位年龄55岁;范围内,29 - 70;男性81%;52%的白人;30%是黑人;(11%拉丁裔),接受cd19靶向CAR - t细胞治疗b细胞淋巴细胞恶性肿瘤。
分析包括19例可评估的患者。
10例(53%)患者获得了cd19靶向CAR-T的客观缓解,其中8例(42%)患者获得了完全缓解。
14名患者(74%)出现细胞因子释放综合征,但研究人员没有报告3级或4级CRS病例。5名患者(26%)出现免疫效应细胞相关神经毒性综合征,包括3名3级症状和1名4级症状。
Barta说:“基于这些初步数据,结果似乎与未感染艾滋病毒的患者报告的结果相同。”
Barta称这些结果令人放心,但他警告说,这些结果必须得到前瞻性的证实,比如一项由amc赞助的研究正处于最后规划阶段。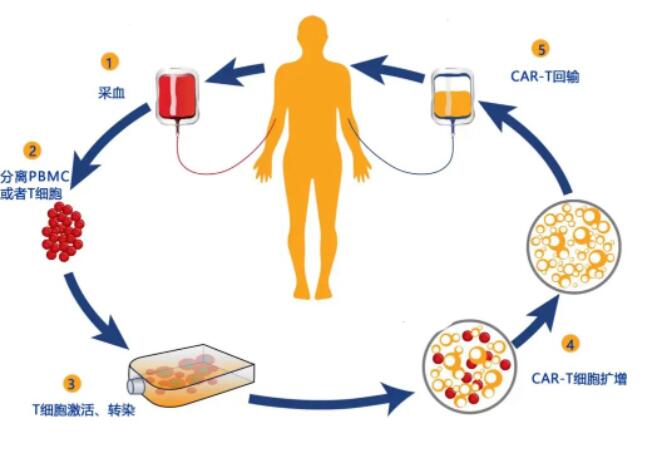
2. “不同的动物”
Barta说,将艾滋病毒感染者排除在新型癌症治疗的临床试验之外一直是一个长期存在的问题,特别是在免疫治疗时代。
四种fda批准的产品治疗某种形式的大b细胞非霍奇金淋巴瘤。在获得批准的注册试验中,没有一个包括艾滋病毒携带者。
Barta说,大多数试验自动取消了那些活动性艾滋病毒感染者的资格,而不考虑其他参数。
他说:“这是一个需要监管当局和进行这些临床试验的人更多关注的问题。”
即使是设计为更具包容性的试验标准,也往往依赖于CD4计数,这可能不是最可靠的衡量标准,因为许多在临床试验中接受CAR-T治疗的人由于先前的癌症治疗而使CD4计数降低。
考虑到大约四分之一的大b细胞淋巴瘤患者——无论是否感染艾滋病毒——无法通过一线治疗治愈,获得大b细胞淋巴瘤的临床试验尤其重要。
Memorial Sloan Kettering癌症中心的主治医师Ariela Noy医学博士专门研究艾滋病毒/艾滋病相关淋巴瘤的治疗,她说,特别高风险人群的额外变量意味着艾滋病毒感染者获得CAR-T治疗的机会增加,这一点不能最小化。
Noy告诉Healio b| Cell Therapy Next:“HIV感染者受到研究人员的大规模歧视,无论是在学术方面还是在制药方面——这是明确的。对这些病人来说,他们因为不再有效的历史原因被排除在外,这是一种讽刺。”
Noy补充说,医生的偏见可能会发挥作用,并且由于耻辱或试图保护研究结果的完整性,行业发起人可能会避免将艾滋病毒感染者纳入他们的试验设计。
加州大学旧金山分校医学名誉教授、Healio b|传染病新闻的首席医学编辑Paul A. Volberding医学博士认为,没有理由禁止艾滋病毒感染者参加癌症临床试验,只要他们在医生的监督下,并且他们的疾病得到了很好的控制。
沃尔伯丁是一名经过培训的癌症专家,他参与了评估艾滋病毒感染的抗逆转录病毒疗法的早期试验,后来成为加州大学旧金山分校艾滋病研究中心的联合主任。
由于艾滋病毒是一种免疫系统疾病,沃尔伯丁说,他理解主办者和研究人员在免疫癌症疗法的注册试验中可能会包括病毒携带者的焦虑。
他说,随着研究人员在新型细胞疗法的后期试验中获得经验,治疗更广泛的临床试验人群,更准确地反映现实世界的实践,将有利于他们。
沃尔伯丁说:“艾滋病毒现在是可以治疗的,感染这种疾病的人基本上可以过上正常的生活。”“由于免疫疗法在治疗恶性肿瘤,尤其是淋巴瘤方面变得如此重要,我认为很明显,hiv阳性患者应该被纳入CAR-T临床试验。”
3. “不要问,不要说”
Noy说,没有一种用于大b细胞非霍奇金淋巴瘤的市售CAR-T产品是专门许可用于HIV患者的。
“但一些制造商却视而不见,”她补充道。“这是一个‘不问,不说’的问题。”
Noy说,从艾滋病毒携带者身上制造CAR - T细胞不会产生安全问题。她补充说,之前的实验表明,在t细胞扩增过程中(CAR-T制造过程的一部分)使用的自体细胞不能复制HIV病毒,这是在受控环境中完成的。
诺华公司生产tisagenlecleucel (Kymriah),这是一种cd19导向的CAR-T治疗复发或难治性b细胞非霍奇金淋巴瘤的成人。
公司发言人告诉Healio b| Cell Therapy Next, tisagenlecleucel在HIV感染者中的安全性和有效性尚未得到证实,来自活动性HIV感染者的粘接细胞将不被接受用于制造这种疗法。
诺华公司在一份声明中说,在接受化疗或抗cd20抗体的患者中,已经报道了与免疫抑制和B细胞耗竭有关的HIV患者的临床已知疾病再激活风险。
Barta说,诺华在这个问题上采取的方法已经过时了,特别是在有效治疗的背景下。
巴尔塔说:“在现代抗逆转录病毒疗法的时代,艾滋病毒感染者已经能够成功地接受自体和异体造血干细胞移植。”“此外,专家的共识是,艾滋病病毒得到良好控制的人可以安全地接受高剂量治疗,包括CD20定向治疗,而不会显著增加风险。”
Kite Pharma上市针对复发或难治性大b细胞非霍奇金淋巴瘤成人的cd19靶向CAR-T axicabtagene ciloleucel (Yescarta)。
Kite的一位女发言人告诉Healio b| Cell Therapy Next,使用阿西卡他格西洛鲁的治疗不受艾滋病毒感染状况的限制,由治疗医生自行决定。
美国食品和药物管理局(FDA)对阿昔卡布基西洛埃尔(axicabtagene ciloleucel)的标签建议医生“在收集细胞用于生产之前,按照临床指南进行艾滋病毒筛查和管理。”
百时美施贵宝(Bristol Myers Squibb)生产的lisocabtagene maraleucel (Breyanzi)是一种cd19靶向CAR-T治疗复发或难治性大b细胞非霍奇金淋巴瘤或一线化疗免疫治疗后早期复发的患者。公司管理人士拒绝了置评请求。
Barta说,缺乏精确的指导,再加上缺乏研究,导致一些保险公司拒绝为商业CAR-T产品提供保险。
他说:“有时我们会遇到保险不批准治疗的问题,因为艾滋病毒患者不包括在注册的CAR-T试验中。”
博罗·德鲁普利奇博士、工商管理硕士——“关怀十字”(Caring Cross)的联合创始人兼执行董事,该组织是一个旨在改善服务不足人群获得先进药物的非营利组织。他是一名训练有素的病毒学家,在基因和细胞治疗方面拥有30多年的经验。他还拥有CAR-T开发和制造方面的专业知识。
他说,他不知道在使用艾滋病毒感染者的细胞的制造过程中有任何安全问题。
“我认为从艾滋病毒感染者身上制造CAR-T细胞没有任何问题。CAR-T细胞产品是使用一次性封闭系统制造的,所以不应该担心交叉污染等问题,”dropuliki告诉Healio | cell Therapy Next。“如果患者在治疗过程中坚持抗逆转录病毒药物治疗,那么我认为他们应该接受与任何接受CAR - T细胞治疗的患者相同的治疗方式。”
4. 填补空缺
尽管有排斥的历史和商业制造商之间的模糊,dropuliki说他相信试验发起人将开始意识到在他们的研究中包括更多不同人群的价值-特别是后期研究。
“让艾滋病毒感染者获得最先进的治疗方法是非常重要的,首先要进行临床试验,然后在获得批准后才能获得治疗,”dropuliki说。“艾滋病毒和淋巴瘤患者是一个需要解决的重要人群。”
他的组织参与了几项试验,与医院合作开发CAR-T候选药物及其制造工艺,目的是在护理点而不是在集中设施生产治疗药物。
目标之一是开发针对HIV和淋巴瘤患者的CAR - t细胞疗法,尽管目前还没有进行临床试验。
诺伊说,转诊医生仍然可以对艾滋病管理和癌症治疗方面的知识进行更新,并对那些疾病控制良好的人进行可能的治疗。
Barta表示同意,他补充说,教育是让艾滋病毒感染者完全获得CAR-T治疗的第一步,现在初步证据表明,CAR-T治疗对这一人群是安全且同样有效的。
他说:“该领域的领导者和大医院的专家有责任领导这些教育工作。”“像艾滋病恶性联盟这样的组织……可以填补这一空白,确保人们不会因为感染艾滋病毒而掉队。”
5. “真正的讽刺”
细胞治疗界几乎一致认为,有必要放宽临床试验排除标准,以帮助扩大CAR-T疗法对艾滋病毒感染者的应用。
Barta和Noy参考了asco -癌症研究之友艾滋病工作组关于现代化临床试验资格标准的建议,该建议于2017年发表在《临床肿瘤学杂志》上。
“HIV感染本身不应该再成为大多数研究的排除标准,”Uldrick和他的同事在他们的建议中写道。
他们补充说:“标准不应该比具有相同疾病或治疗史的未感染艾滋病病毒的患者更严格。”
Barta同意该小组的总体结论,并说在临床试验选择的背景下,HIV感染应该被视为一种共病,而不是一个全面的排除标准。
“我们不会让任何不受控制的心力衰竭患者进行临床试验,这是完全有道理的,”巴尔塔说。“同样,我们不应该让任何感染失控的人——包括艾滋病毒——进行临床试验,因为我们要确保安全仍然是我们的首要关注点。”
尽管工作组提出了建议,但许多试验——尤其是那些评估免疫肿瘤学药物的试验——仍然将艾滋病毒感染者排除在外。Barta说,这些试验往往有相当不切实际的纳入标准,比如相对较高的CD4计数。
诺伊是工作组成员之一,他对在执行建议方面缺乏进展表示遗憾。
她说:“当我们做到这一点时,我感到非常自豪,我真的很荣幸有机会对人们的生活产生影响。”“这些努力没有带来任何改变,这真是一个真正的讽刺。”
并非所有艾滋病毒感染者都有资格接受CAR-T试验或标准治疗;然而,诺伊说,参与应该基于患者的整体生物学,而不是艾滋病毒状况或任何其他单一因素。
AMC正在其即将进行的前瞻性研究AMC-112中采用这种方法,该研究将检验axicabtagene ciloleucel在成人HIV和复发或难治性b细胞非霍奇金淋巴瘤患者中的安全性和有效性。
该试验由NCI和Kite Pharma共同赞助,将是CAR-T的第一个一期前瞻性研究,其中包括HIV患者。
AMC成员Noy说,排除标准将基于生物学相关因素,并考虑到工作组的许多建议。
“我们会问重要的问题,”她说。
它们将包括患者最近是否有机会性感染,为参与建立合理和安全的病毒载量限制,并评估未来的入组者是否坚持他或她的抗逆转录病毒治疗方案。
Noy说:“这些问题的答案可以预测艾滋病毒患者癌症治疗的异常不良结果,因此我们将所有艾滋病毒患者纳入我们的研究是没有意义的。然而,这些都是生物学问题,没有一个是歧视性的。”
【责任编辑:阿杰 邮箱:xjpop@vip.qq.com】



