
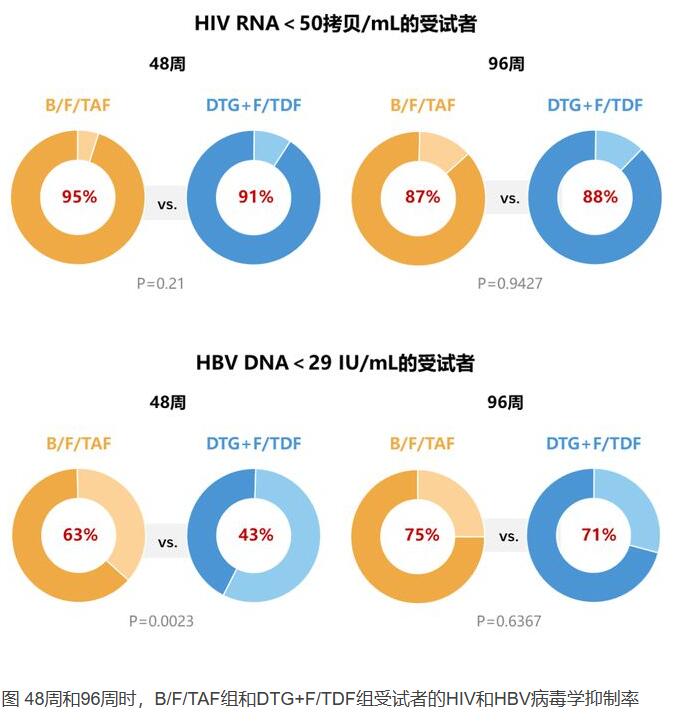
我们借鉴作为主要研究者的中国医学科学院北京协和医院的李太生教授对这一研究的理解,为大家解读这一重要研究结果,并深入探讨HIV/HBV合并感染者ART方案的考量因素。 ALLIANCE研究结果 ALLIANCE研究在亚洲、欧洲、北美洲多个国家及地区的46个门诊中心进行,2018年5月30日至2021年3月16日间,招募了243例血浆HIV RNA≥500拷贝/mL、血浆HBV DNA≥2000 IU/mL的18岁及以上的初治合并感染者。受试者以1:1的比例被随机分配到B/F/TAF组(121例)或DTG+F/TDF组(122例)。 受试者绝大部分(88%)来自亚洲,30%的受试者HIV RNA>100,000拷贝/mL,晚发现者的比例较高,40%的CD4细胞计数<200个/μL,44%的谷丙转氨酶(ALT)高于正常值上限(男性25 U/L,女性35 U/L),HBV病毒载量较高,52%的HBV DNA≥8 log10 IU/mL,78%为基线HBeAg阳性。 病毒学结果方面,96周时,HIV RNA的抑制率延续了48周的结果趋势,B/F/TAF组和DTG+F/TDF组的HIV病毒学抑制率分别为87%和88%,具有非劣效性。HBV病毒学抑制率分别为75%和70%。24-96周内,B/F/TAF组的HBV病毒学抑制率数值上高于DTG+F/TDF组,且在48周和72周时具有统计学差异。本研究中的HIV病毒学抑制率与此前含BIC和DTG的方案相关研究结果一致,HBV病毒学抑制率与3期临床研究中HBeAg阳性的单一HBV感染者大致相似。
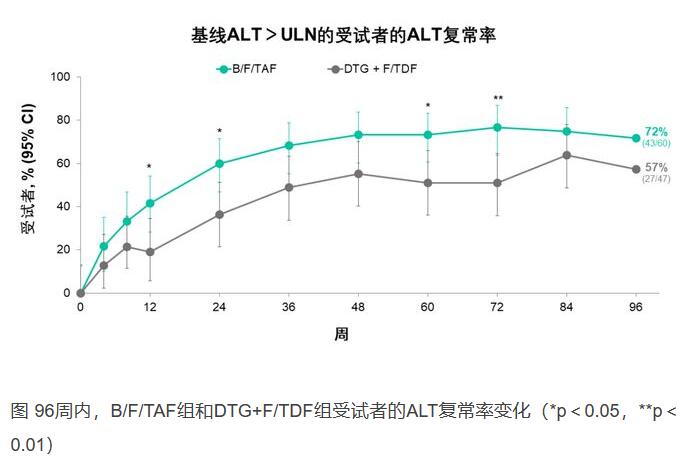
生化学结果方面,96周时,两组的ALT复常率不具有统计学差异,B/F/TAF组为72%,DTG+F/TDF组为57%(p=0.13),但在所有随访时间点上,B/F/TAF组的ALT复常率在数值上均高于DTG+F/TDF组,中位ALT和谷草转氨酶(AST)下降也更多。
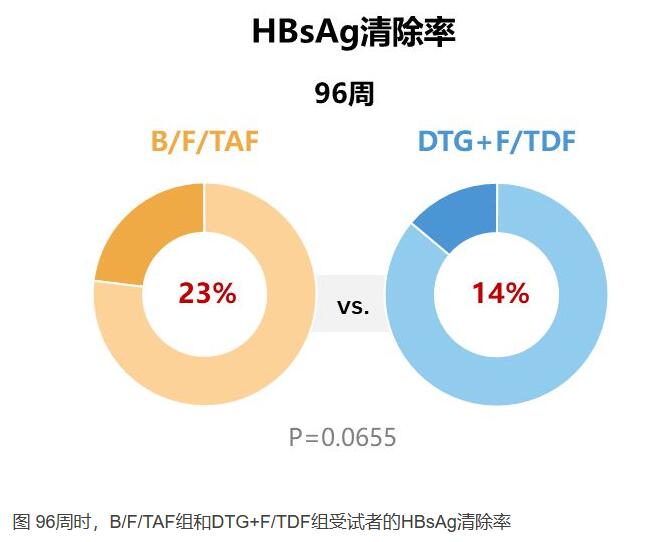
HBV血清学结果方面,96周时,B/F/TAF组的HBsAg清除率为23%,在数值上高于DTG+F/TDF组(14%),并且在24周和36周时具有统计学差异。HBsAg清除是慢性乙型肝炎患者的临床治愈指标,显著降低HBV感染者失代偿期肝硬化、肝衰竭等终末期肝病和肝细胞癌的风险,改善感染者的远期结局[17]。96周时,B/F/TAF组的HBeAg清除率为38%,显著高于DTG+F/TDF组的20%(p=0.0064)。
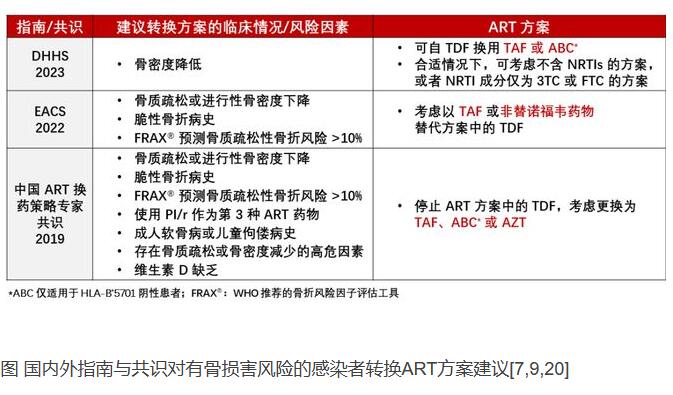
安全性结果方面,B/F/TAF和DTG+F/TDF均具有较高的安全性,大多数不良事件(AE)为1-2级,3或4级AE(14.0% vs. 15.6%),以及药物相关AE(24.0% vs. 27.0%)的发生率相近。 耐药性结果方面,B/F/TAF组没有出现治疗中耐药,DTG+F/TDF组出现1例治疗中耐药,发生耐药的受试者报告对治疗依从性差,24周时检测到K70E突变,36周时检测到M184V/I突变,随后重新获得病毒学抑制。 这项研究表明,对于HIV/HBV合并感染,B/F/TAF相比DTG+F/TDF在HIV病毒学抑制方面具有非劣效性,对HBV的抑制率、ALT复常率和HBsAg清除率方面有更高的趋势,这些结果为HIV/HBV合并感染者的治疗方案选择提供了非常重要的临床依据。 HIV/HBV合并感染者的 治疗重要考量因素 HIV/HBV合并感染者在选择治疗方案时,除了强效的双重病毒学抑制,还有其他的重要因素需要纳入考量。 肝脏安全性方面,合并感染者的肝损伤风险更高,选择ART方案时需将药物的肝脏安全性纳入考量,整合酶抑制剂(INSTI)整体的肝脏安全性较高,而依非韦伦(EFV)和洛匹那韦/利托那韦(LPV/r)等易引起肝损伤,在肝功能受损感染者中应慎用[9]。 骨骼和肾脏安全性方面,合并HBV感染是接受ART的HIV感染者发生慢性进行性肾病的独立预测因素,合并感染者的慢性肾病发生率是HIV单一感染者的6倍[18]。 TAF相比TDF对肾脏和骨骼的影响更小,瑞士的一项前瞻性队列研究显示,伴肾功能损伤的经治HIV/HBV合并感染者由含TDF的方案转换为含TAF的方案12个月后肾功能指标显著改善,基线时eGFR为60-89 mL/min/1.73m2的参与者提高了3.2 mL/min/1.73m2,eGFR<60 mL/min/1.73m2的提高了6.2 mL/min/1.73m2[19]。各大指南和共识为使用含TDF方案感染者有骨损害风险需转换治疗方案的情况及可转换方案提供了较为一致的建议。
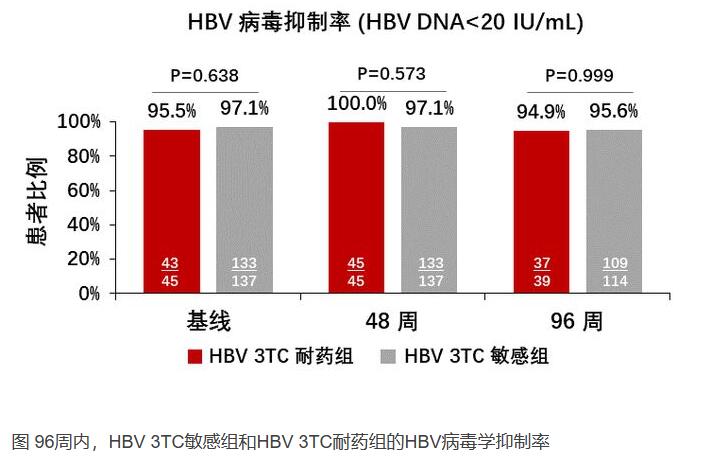
耐药性方面,国内外指南推荐HIV/HBV合并感染者使用含两种同时具有抑制HIV和HBV作用的NRTI的三联方案,以避免单一NRTI诱导的HBV耐药,不合适的ART方案可能诱导高HBV耐药率,中国广西的一项多中心横断面研究显示,未接受抗HBV治疗的合并感染者中,ART经治感染者存在拉米夫定(3TC)HBV耐药突变的比例为76.5%,未接受ART的仅为1.4%,在耐药经治者中,85%有仅含3TC一种抗HBV活性药物方案一年以上的治疗史[21]。 存在耐药突变的HIV/HBV合并感染者在选择ART方案时需包含耐药屏障高的NRTI。中国台湾的一项回顾性研究对182例由含TDF方案转换为含TAF方案的合并感染者的疗效进行分析,其中45例(24.7%)参与者感染的HBV毒株对3TC耐药,转换TAF后96周,耐药组和敏感组的HBV病毒学抑制率(HBV DNA<20 IU/mL)均较高[22]。这表明,存在3TC耐药突变,不会影响含TAF的方案对HBV病毒学的抑制。
HBV再激活方面,HBV再激活可自发发生,常由癌症、免疫性疾病或移植相关的免疫抑制治疗引起。持续接受ART的HIV/HBV合并感染者的HBV再激活风险较小,但停用含抗HBV活性的药物时,HBV再激活风险显著升高。 在HBsAg阴性的HIV感染者中存在HBV隐匿感染的可能,HIV感染者中隐匿性乙型肝炎的流行率高于一般人群(16.26% vs. 0.82%)[23]。在这种情况下,转换为不含对HBV有高耐药屏障的NRTI或仅含有一种NRTI的二联药物ART方案均有引起HBV再激活的可能。意大利ICONA队列研究显示,101例HBsAg阴性/HBcAb(HBV核心抗体)阳性、HIV病毒学抑制>12个月的合并感染者转换为不含TDF或TAF的方案后12个月,HBV再激活率高达40%,转换至含3TC方案的也达到32.1%,与转换为不含抗HBV活性药物的ART相比没有显著差异。可见,不含TDF和TAF的ART方案与HBV再激活相关[24]。 另一项多中心队列研究也发现,单一HBcAb阳性的HIV感染者转换为基于3TC的二联方案后,HBcAb阳性组在所有时间点上HIV RNA低于检测下限的比例均显著低于HBcAb阴性组(第24个月:64.7% vs. 87.8%,p<0.0001;第36个月:62.7% vs. 86.8%,p=0.011;第48个月:57.2% vs. 86.1%,p=0.021)。HBcAb阳性使随访期间HIV病毒学反弹显著增加54%(p=0.004)[25]。
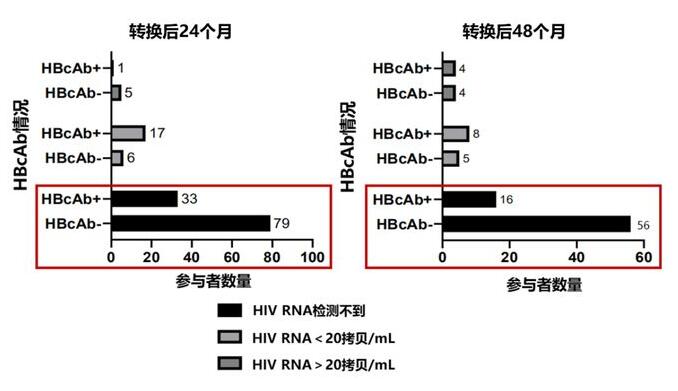
图 转换方案后24个月和48个月,HBcAb阳性组和HBcAb阴性组的HIV RNA水平
类似的,一项病例系列研究显示,38例HBcAb阳性/HBsAg阴性的HIV感染者转换为不具有抗HBV活性的长效卡替拉韦/利匹韦林(CAB/RPV)方案后,3例(7.9%)发生了HBV病毒血症[26]。 对于接受抗肿瘤或免疫抑制治疗的群体来说,TAF可有效预防HBV再激活,日本的一项前瞻性多中心研究显示,106例接受抗肿瘤或免疫抑制治疗的HBV携带者接受6个月的TAF预防性治疗,没有发生HBV再激活、HBV再激活相关肝炎,或因HBV再激活或TAF相关不良事件停药[27]。 总的来说,相比单一HIV感染者,HIV/HBV合并感染者具有较差的长期预后,在启动治疗时应首选含TAF/TDF+FTC/3TC的三联ART方案,以同时抑制HIV和HBV,且更需快速启动ART。ALLIANCE研究显示,HIV/HBV合并感染者使用B/F/TAF,可有效抑制 HIV 和 HBV 病毒复制,且安全性佳,可作为合并感染者的首选方案。同时,B/F/TAF也是指南推荐的唯一可用于HIV/HBV合并感染治疗且唯一可作为ART快速启动的复方单片制剂。 研究者点评 HIV/HBV合并感染者发生肝脏合并症的风险显著升高,疾病进程加快,在HIV感染者的临床管理中,应重视筛查HBV感染,对于HBsAg阴性/HBcAb阳性的感染者也需要考虑隐匿性HBV感染的可能,在治疗方面需要需加速启动ART,使用强效的双重病毒学抑制的ART方案。 在国内外指南推荐的一线ART方案中,INSTI+2 NRTI三联方案具有高肝脏、骨骼和肾脏安全性,且适用于快速启动,不易诱发HBV耐药和HBV再激活,而DTG/3TC二联方案不适用于合并感染者,且在隐匿性HBV感染者中HBV再激活风险显著升高,进而可能干扰HIV病毒学抑制。在启动治疗后,应长期监测HBV DNA、肾功能、骨密度和肝脏合并症进展,以及时调整ART方案和/或开展辅助治疗,也是HIV/HBV合并感染者的长期治疗成功的关键因素。 ALLIANCE研究是首个比较包含TAF与包含TDF的ART方案治疗HIV/HBV合并感染者的随机对照临床研究。除了高病毒学抑制率外,需要格外关注的是较高的HBsAg清除率,HBsAg清除是慢性乙型肝炎临床治愈的指标,能显著减少肝硬化及肝细胞癌等肝脏不良结局的发生率,是目前慢乙肝治疗的理想终点。HBsAg清除在HBV单一感染者中通常较为罕见,单一HBV感染者接受TAF治疗的临床试验中,96周时的HBsAg清除或血清转换率仅为1%甚至更低[28],ALLIANCE研究受试者基线时多为HBeAg阳性,基线HBV DNA载量较高,且有将近一半的受试者ALT异常,这些基线特征通常是慢乙肝患者HBsAg阴转的不利因素,在此情况下,ALLIANCE研究达到的高HBsAg清除率更具临床意义。 高HBsAg清除率的原因引发思考,一方面,HIV/HBV合并感染者较HBV单一感染者HBsAg清除率更高的原因,ALLIANCE研究受试者多来自亚洲,年龄较轻,多为HBeAg阳性,病毒载量较高,大多处于HBV感染自然史中的免疫耐受期,而HIV诱导的免疫紊乱可能打破宿主的免疫耐受,含TAF方案的高效ART快速清除病毒的同时免疫重建,强有力地帮助HBV的免疫清除。此前也有多项研究发现HIV/HBV合并感染者有较高的HBsAg清除率,HBsAg清除与基线CD4细胞计数及治疗后CD4细胞增加相关[29-31],均表明免疫重建在HBsAg清除中的重要作用。另一方面,B/F/TAF组较DTG+F/TDF组HBsAg清除率更高的原因,由于药代动力学的差异,TAF在肝脏细胞较TDF产生的活性产物TFV-DP更加富集,从而可能更快和更强效抑制HBV复制,在免疫重建的联合作用下,B/F/TAF组从而达到非常高的HBsAg清除率。 综上所述,HIV/HBV合并感染者经历了HBV免疫耐受的打破及治疗后免疫重建,宿主HBV免疫的破而后立有助于HBsAg清除;这个连续的过程(打破耐受+免疫重建)也存在于淋巴瘤患者化疗后干细胞移植中,既往研究报道了该类患者中HBsAg清除案例[32]。 结合已知的长期骨骼和肾脏安全性优势,ALLIANCE研究为合并感染者接受复方单片制剂B/F/TAF的临床获益提供了支持,为合并感染者治疗后HBsAg清除率较高提供了高质量的证据,标志着对于HIV/HBV合并感染者优化治疗定义的重要一步。仍有许多值得探讨的问题,如HBsAg清除的感染者能否持续维持HBV功能性治愈?HBsAg血清转换者有效抗体滴度持续时间?其他HBV感染的血清标志物(HBV cccDNA,HBV RNA,HBcrAg)的抑制情况,对于合并感染者HBsAg清除的长期临床获益与HBV单一感染者是否有差别?合并感染者高HBsAg清除率对HBV单一感染者追求临床治愈研究的启发,均为这一领域未来研究非常有意义的方向。






